12/12/2018
Encuentran un nuevo mecanismo de transporte de nanomateriales a través de la membrana celular
Una investigación de la URV muestra que es posible controlar el transporte de nanomateriales a través de la membrana celular, ajustando la tensión

Una investigación de la URV muestra que es posible controlar el transporte de nanomateriales a través de la membrana celular, ajustando la tensión
Los efectos biológicos y la toxicidad de los nanomateriales que interactúan con las células cada vez se entienden más, pero hay que profundizar en los mecanismos por los cuales los nanomateriales pueden atravesar las membranas de los lípidos. Además, de los mecanismos de transporte común como por ejemplo la endocitosis -por el cual célula capta material del espacio extracelular hacia su interior-, que ya se han discutido con profundidad, los principios de la física indican que pueden tener otras. Siguiendo esta hipótesis, el equipo de físicos teóricos de la Universitat Rovira i Virgili de Tarragona, encabezado por el investigador Vladímir Baulin, ha diseñado un proyecto de investigación para investigar la interacción entre las membranas lipídicas y los nanotubos de carbono. En simulaciones computacionales, los investigadores han estudiado lo que denominan “modelo de membrana lipídica”, formada por sólo un tipo de lípido. El equipo de Baulin ha observado que, según sus cálculos, los nanotubos de carbono ultracortos se pueden insertar perpendicularmente en la membrana celular formada por bicapa lipídica, las barreras que protegen la célula.
Han constatado que estos nanotubos quedan atrapados en la membrana celular, cosa que está generalmente aceptada por la comunidad científica. Sorprendentemente, pero, cuando han estirado la membrana celular de su modelo y han insertado los nanotubos que estaban atrapados en la bicapa, de repente han empezado a escaparse por los dos lados. Esto significa que es posible controlar el transporte de nanomateriales a través de la membrana celular ajustando la tensión.
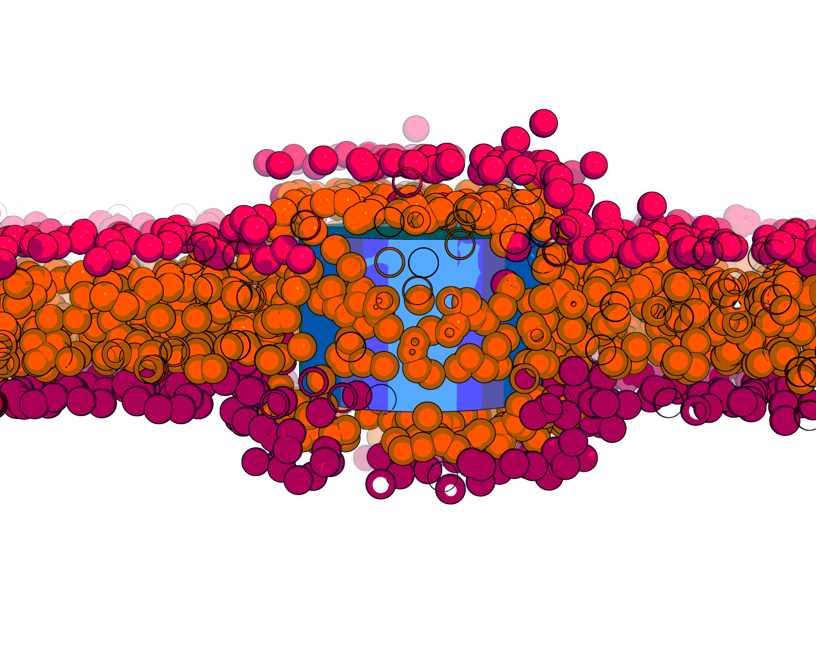
En este punto Baulin ha contactado con el investigador Jean-Baptiste Fleury, de la Universidad de Saarland (Alemania), para confirmar este mecanismo y para hacer un estudio experimental de este fenómeno de transporte favorecido por la tensión. Fleury y su equipo han diseñado un experimento de microfluidos con una bicapa fosfolipídica muy controlada, un modelo para membranas celulares y con nanotubos de carbono ultracortos (10 nm de longitud). Los nanotubos tenían una monocapa lipídica adsorbida que garantiza que se dispersen de forma estable e impide que se agrupen. Utilizando una combinación de microscopio fluorescente y medidas electrofisiològicas al mismo tiempo, el equipo de Fleury ha podido seguir los nanotubos individuales que atravesaban la bicapa y aclarar el recorrido desde el punto de vista molecular. Tal como se había previsto durante las simulaciones, han observado que los nanotubos que se han insertado en la bicapa mediante la disolución del lípido cubren la membrana lipídica. Cuando se aplicaba una tensión de 4mN/m a la membrana, los nanotubos se escapaban espontáneamente en tan solo unos cuántos milisegundos. Ahora bien, si la tensión era menor, los nanotubos se quedaban atrapados dentro de la membrana. Por lo tanto, este nuevo mecanismo permite un control preciso del transporte a través de las membranas.
Desde otro punto este descubrimiento en el que pequeños nanotubos pueden pasar a través de las barreras que protegen las células –la bicapa lipídica– puede plantear dudas sobre la seguridad de los nanomateriales en la salud pública y estimular la búsqueda de nuevos sistemas mecánicos para controlar la administración de medicamentos.
Referencia bibliográfica: Guo, Y.; Werner, M.; Seemann, R.; Baulin, V. A.; Fleury, J.-B. Tension-Induced Translocation of Ultra-Short Carbon Nanotube through a Phospholipid Bilayer. ACS Nano 2018. https://doi.org/10.1021/acsnano.8b04657.
